|
|
|
| stałym | |
| ciekłym | |
| lotnym (czyli jako gaz, lub para) |
Fazę ciekłą i gazową łącznie określa się mianem płynu (choć dochodzą tu jeszcze dodatkowe stany - np. kolid).
Cechy ciał w trzech podstawowych stanach skupienia są następujące:
| w stanie stałym - ciało posiada określony kształt i
samorzutnie, a także mimo działania niewielkich sił ten stan
zachowuje. Ciała w stanie stałym charakteryzują się sprężystością.
Ściśliwość ciał stałych jest szczątkowa. Typowo dzielimy ciała stałe na: - krystaliczne - patrząc od strony mikroskopowej posiadające uporządkowane szeregi cząsteczek, lub atomów (jest to tzw. struktura dalekiego zasięgu) - bezpostaciowe - ciała te w budowie mikroskopowej przypominają ciecz, tzn. brakuje długich szeregów atomów, czy cząsteczek. | |
| w stanie ciekłym - ciało w warunkach działania siły grawitacji gromadzi się dolnej części naczynia, przenika przez pory i szczeliny, nie ma stałego kształtu. Posiada natomiast powierzchnię charakteryzującą się pewnego rodzaju niewielką sprężystością. Patrząc od strony mikroskopowej, ciecze posiadają pewną regularność ułożenia atomów i cząsteczek w zasięgu kilku - kilkunastu odległości międzatomowych. Jednak brakuje tu struktury dalekiego zasięgu. Ciecze są bardzo słabo ściśliwe (właściwie prawie nieściśliwe) | |
| w stanie gazowym - ciało rozprzestrzenia się w całej objętości naczynia. Gaz wywiera ciśnienie na otaczające go przedmioty, jest ściśliwy łatwo się miesza z innymi substancjami lotnymi. |
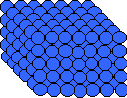
Schematyczna budowa mikroskopowa w trzech stanach skupienia
| ciało stałe krystaliczne | ciecz, lub ciało stałe bezpostaciowe | gaz |
 |
 |
 |
Egzotyczne stany materii, czyli szersze spojrzenie na pojęcie stanu skupienia
W dzisiejszych czasach nauka powoli odchodzi od mówienia o prostym podziale na trzy stany skupienia materii. Co prawda otaczające nas ciała rzeczywiście jakoś z grubsza da się przypisać do wspomnianych trzech stanów, to jednak bliższe przyjrzenie się temu jak organizują się atomy i cząsteczki różnych substancji skłania do wniosku, że form istnienia materii dałoby się wyróżnić znacznie więcej.
Plazma, czyli gaz zjonizowany
Jedną z dodatkowych, sztandarowych form istnienia materii jest plazma. Tym słowem określa się gaz, który został podgrzany tak mocno, że atomy ulegną jonizacji, cały "gaz" rozpadnie się na oddzielnie poruszające się elektrony i osobne jon (w skrajnych przypadkach mogą to być wręcz jądra atomowe, czyli jony pozbawione zupełnie elektronów). Plazmę dość często uważa się za czwarty, lotny stan skupienia materii, przypominający gaz, ale mający nowe, szczególne właściwości.
Koloidy
Ciekawym stanem materii jest koloid. Tak nazywamy dokładne rozpylenie, wymieszanie, rozproszenie cząsteczek jednej substancji w innej. Koloid różni się od roztworu tym, że w tym pierwszym przypadku nie ma wymieszania pojedynczych cząsteczek, ale nieco większe ich skupiska - pyłki, cząsteczki zawiesiny. Są one jednak na tyle małe, że nie da się ich dojrzeć nie tylko gołym okiem, ale także przez lupę, czy nawet słabsze mikroskopy. Do kolidów zaliczamy tzw. zole, aerozole, piany, emulsje, pirozole (aerozole stałe).
Różne postacie fazy stałej
Poza tym nawet jeślibyśmy skupili się tylko na znanych stanach skupienia - np. fazie stałej, to okaże się, że ta sama substancja, w zależności od warunków może przyjmować bardzo różne postacie. Pod wpływem dużych ciśnień i temperatur atomy i cząsteczki układają się w różne formy krystaliczne, przez co jedna i ta sama substancja może wystepować w formach różniących się znacznie gęstością, wytrzymałością, kolorem, czy innymi właściwościami.
Egzotyczne ciecze
Szczególnie ciekawymi formami materii są ciecze kriogeniczne, czyli ciecze powstałe ze skroplenia substancji, które w normalnych warunkach są w stanie gazowym. Najbardziej chyba znaną cieczą kriogeniczną jest Hel II. Ta faza helu, osiągana w temperaturze prawie zera bezwzględnego ma niezwykłe właściwości - np. nadciekłość.
Mnogość postaci wody
Jako przykład złożoności materii można podać wodę, a w szczególności jej stałą fazę - lód. Eskimosi podobno potrafią wyróżnić aż kilkadziesiąt różnych postaci lodu, ale większość z nich nawet nie ma pojęcia o formach tej substancji dostępnych w kosmosie, czy w laboratoriach fizyków. Zwykły lód jest lżejszy od wody, ale istnieją formy lodu, które są znacznie cięższe - mają gęstość nawet dwukrotnie przekraczającą gęstość zwykłej wody w warunkach normalnych. Więcej informacji o różnych postaciach lodu można (po angielsku) znaleźć na stronie http://www.lsbu.ac.uk/water/phase.html .
Dodatkowe informacje o stanach skupienia znajdują się w rozdziałach
| Energia topnienia | |
| Energia parowania | |
| Temperatura przejścia fazowego |